化学試験に合格する方法
著者:
Roger Morrison
作成日:
3 9月 2021
更新日:
1 J 2024

コンテンツ
この記事の内容:良い学習習慣を開発する原子構造を理解する化学反応を予測する化学に数学を適用する化学の言語を使用する
一般的な化学コースで成功するには、この主題の基礎を理解し、簡単な計算を行い、電卓を使用してより複雑な操作を実行し、本当に異なることを学ぶ準備ができている必要があります。化学は物質とその特性を研究する科学です。私たちの周りのすべては、あなたが飲む水や呼吸する空気の性質など、あなたが全く自然だと考えるかもしれない最も基本的なものでさえ、化学に関係しています。あなたの周りの世界を、原子レベルでさえ理解することになると、新しい知識にオープンでいてください。化学との最初の接触はやりがいがあり、刺激的です。
ステージ
パート1優れた学習習慣の開発
-

先生を知ることを学ぶ。 化学のクラスで成功し、クラスでより良い成績を得るには、時間をかけて先生に会い、理解できないことを彼と共有してください。- 多くの教師には学習ガイドがあり、必要に応じて授業時間外に学習者を受け入れます。
-

研究グループを結成または参加します。 化学コースが非常に複雑だと思っても恥ずかしくないでください。これはほとんどすべての人にとって難しい課題です。- グループに参加すると、一部のメンバーは他のメンバーよりもコースの一部を見つけやすくなり、全員と学習方法を共有できます。タスクを分割します。
-

章を読んでください。 化学の教科書は、常に最も刺激的な本とは限りません。それでも、与えられた古典を読み、理解できない部分を強調するために時間をかける必要があります。理解できない質問や概念のリストを作成してください。- 後でこれらのわかりにくい部分をもう一度読んでみてください。それでも理解できない場合は、研究グループ、教師、または助教授と話し合ってください。
-

調査の質問に答えてください。 勉強しているすべてのドキュメントに圧倒されているような印象を受けたとしても、考えているよりも多くの概念を覚えている可能性があることを知っておいてください。章の最後にある質問に答えてください。- ほとんどの教科書には、正しい答えを見つける方法に関する他の情報が記載されています。これにより、推論で見落としたことを確認できます。
-

図、写真、および表を調べます。 教科書には、覚えておくべき重要な要素をよりよく理解するのに役立つビジュアルがよく表示されます。- それらに付随する写真とキャプションをよく見てください。これは、いくつかの概念を理解するのに役立ちます。
-

コースを登録する許可を求めます。 ノートにメモを取り、同時にボードに書かれているもの、特に化学のような複雑なコースを見るのは難しいです。 -

古い証明と古いマニュアルを用意してください。 ほとんどの学校では、学習者が試験の準備に役立つように古い試験の正当性を認めています。- 答えを単に暗記することは避けてください。化学では、同じ質問に異なる用語で回答できるようにするには、概念を理解する必要があります。
-

オンラインヘルプリソースをご覧ください。 所属機関の化学部門が提供するリンクまたはオンラインリソースをご覧ください。
パート2原子構造を理解する
-

最も基本的な構造から始めます。 化学試験に合格するには、物質または質量を持つすべてのものを構成する基本要素を理解する必要があります。- 化学の最も基本的な要素、つまりラトームの構造を理解することが、この分野を理解する最初のステップです。クラスで取り上げるすべてのトピックは、この基本情報の拡張です。原子化学を理解するのに必要な時間をかけてください。
-
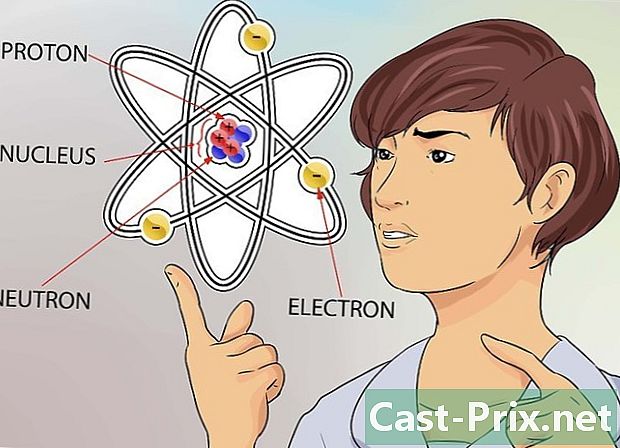
ダトメの概念を理解する。 ラトームは、ガスなど、私たちが常に見ることのできないものを含む、すべての物質の最小の構成要素であると考えられています。しかし、小さな原子でさえ、その構造を構成するさらに小さな粒子で構成されています。- 原子は、中性子、陽子、電子で構成されています。ラトームの中心は核と呼ばれ、これは中性子と陽子で構成されています。電子は、惑星が太陽の周りを公転するように、ラトームの周りに引き寄せられる粒子です。
- アトムのサイズは信じられないほど小さいですが、比較のために、あなたが知っている最大のスタジアムを考えてみてください。この段階を原子と見なすと、核はフィールドの中央に置かれたエンドウ豆と同じくらい大きくなります。
-
要素の原子構造を理解します。 用語 要素 は、他の基本的な要素に分解できない自然に発生する物質として定義され、その最も単純な形式です。要素はdatomesで構成されます。- 要素に存在する原子はすべて同じです。これは、その原子構造内の各要素が既知の一意の数の中性子と陽子を持っていることを意味します。
-
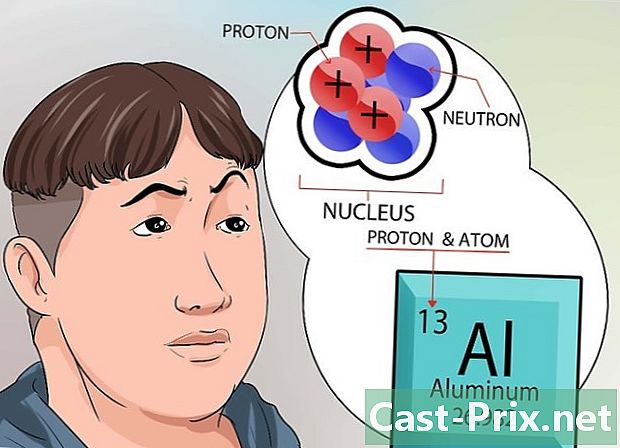
カーネルの詳細をご覧ください。 核の中にある中性子は中性の電荷を持っています。一方、プロトンには正の電荷があります。元素の原子番号は、その核に存在する陽子の数に正確に対応しています。- 元素の陽子の数を知るために数学的な計算を行う必要はありません。この値は、周期表の各要素の各ボックスの上部に示されています。
-
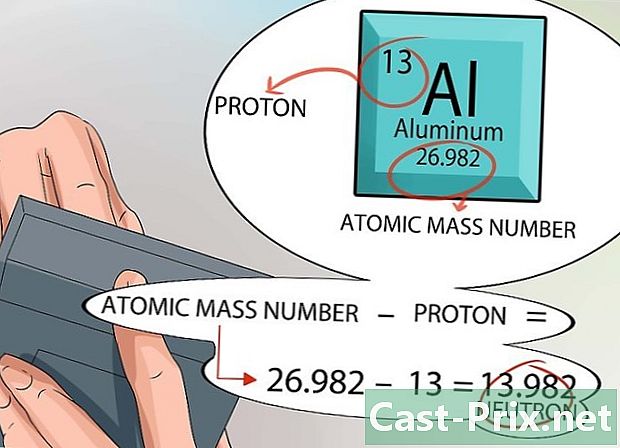
核内の中性子数を計算します。 この目的のために、周期表で提供される情報を使用できます。各元素の原子番号は、核内の陽子の数に等しくなります。- 原子質量は周期表の各ボックスに示され、元素名のすぐ下にあります。
- 陽子と中性子だけが核内にあることに注意してください。周期表を使用すると、陽子の数と化学元素の原子質量を知ることができます。
- この時点で、計算は非常に簡単です。原子の質量から陽子の数を引くだけで、その元素のラトーム核内の中性子の数がわかります。
-
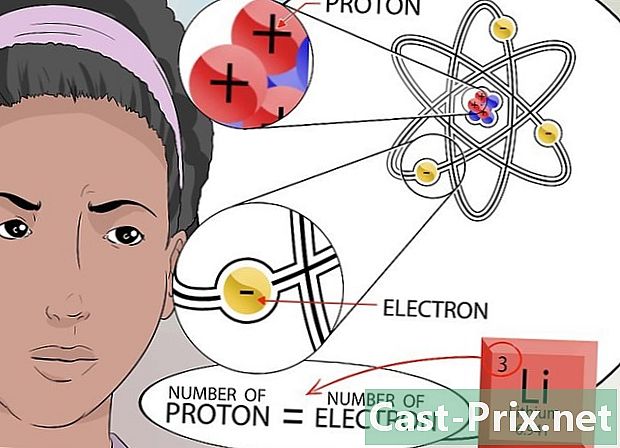
電子の数を決定します。 反対の要素が正しいことを忘れないでください。電子は、惑星が太陽の周りを公転するように、核の周りを公転する負に帯電した粒子です。核に引き付けられる電子の数(負の電荷を持つ)は、核に存在する陽子の数(正の電荷を持つ)に依存します。- ラトームの総電荷はゼロであるため、すべての正電荷と負電荷のバランスを取る必要があります。このため、電子の数は陽子の数に等しくなります。
-
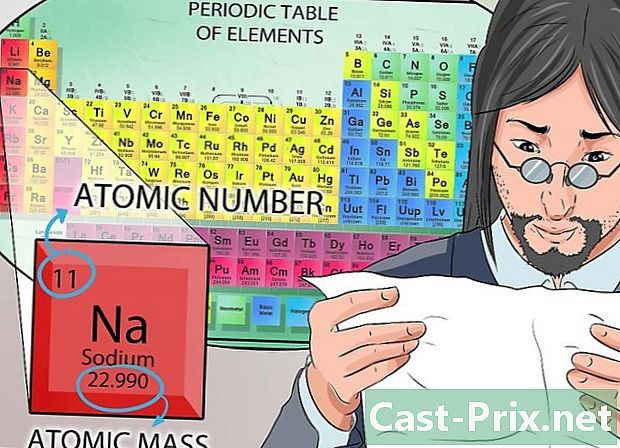
周期表を観察します。 化学元素の特性を理解できない場合は、時間をかけて周期表に記載されているすべての情報を確認してください。最も重要なことは、チャートを注意深く調べることです。- このチャートを理解することは、化学クラスの最初の部分を成功させるために不可欠です。
- 周期表は元素のみで構成されています。各2つは、1つまたは2つのシンボルで表されます。シンボルは、要素を一意に識別します。たとえば、シンボル ナ 常にナトリウムラトムを意味します。化学元素のフルネームは通常、シンボルの下に書かれています。
- シンボルの原子番号は、その上に印刷された番号で表されます。原子番号は核内の陽子の数に等しい。
- 記号の下の数字は原子質量に対応しています。これを忘れないでください。原子の質量数は、核に含まれる陽子と中性子の合計に等しくなります。
-
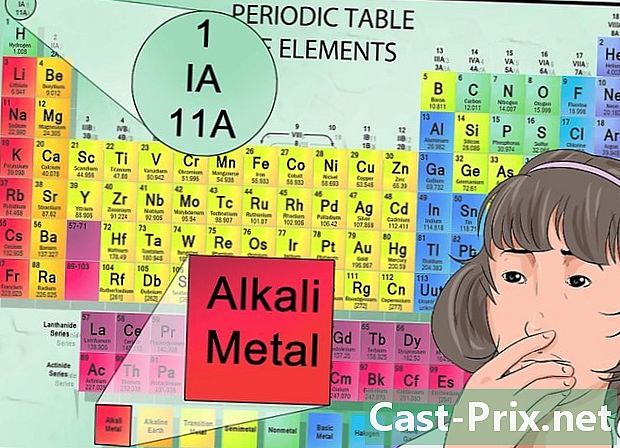
周期表を解釈します。 周期表には、各列の色や、左から右、上から下への要素の位置など、多くの情報があります。
パート3化学反応の予測
-

化学式のバランスをとります。 化学では、要素が互いにどのように反応するかを予測する必要があります。つまり、化学反応のバランスを取ることができなければなりません。- 化学式では、試薬は左側にあり、その後に反応生成物を示す右向きの矢印があります。そして、方程式の両側の要素はバランスが取れていなければなりません。
- たとえば、試薬1 +試薬2→製品1 +製品2。
- 錫の記号を使用した例を次に示します。記号はSnです。二酸化スズ(SnO2)と気体状の水素(H2)を組み合わせます。方程式はSnO2 + H2→Sn + H2Oです。
- ただし、試薬の量は製品の量と等しくないため、この式はバランスが取れていません。反応の右側よりも左側に1つ多くの酸素原子があります。
- 簡単な数学的計算を使用して、左側に2つの水素ユニットを配置し、右側に2つの水分子を配置することにより、方程式のバランスを取ることができます。平衡化された反応は、SnO2 + 2 H2→Sn + 2 H2Oになります。
-
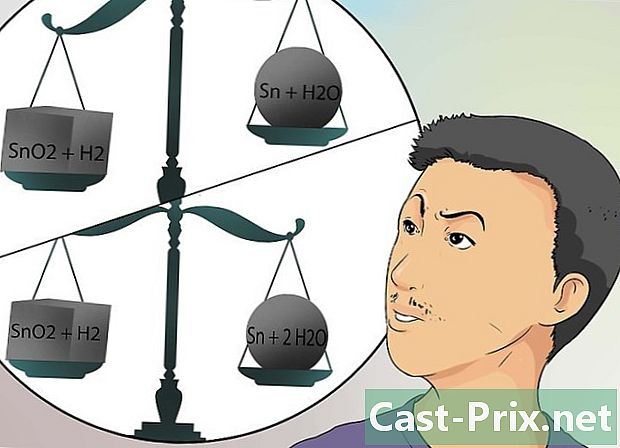
方程式の考え方を変えてください。 化学反応のバランスをとるのが難しい場合は、レシピのどの部分を想像してください。ただし、レシピの最終製品を多少なりとも調整する必要があります。- 方程式は、方程式の左側に成分を提供しますが、用量に関する情報は提供しません。ただし、この方程式を使用すると、製品として得られるものを知ることができ、常に数量は省略されます。そして、あなたはそれらを見つけなければなりません。
- 常に上記の例(SnO2 + H2→Sn + H2Oの例)を使用して、この反応(またはレシピの公式)が機能しない理由を検討してください。式の両側のスズ(Sn)の量は等しく、水素(H2)の量も同じです。ただし、左側には2つの酸素原子があり、右側には1つの原子しかありません。
- 式の右側を変更して、H2Oの2つの分子(2 H2O)があることを示します。前の2番 H2O これは、この分子のすべての原子が現在2倍になっていることを意味します。現在、酸素の量は釣り合っていますが、水素の量ではありません。なぜなら、右側には左側よりも多くの水素があるからです。このため、方程式の左側に戻る必要があります。 H2成分の量を変更し、H2の前に係数2を配置して2倍にします。
- そして、ここであなたは、方程式の両側で成分のすべての用量のバランスをとっています。レシピの材料は、得られる製品と同じです(したがってバランスが取れています)。
-
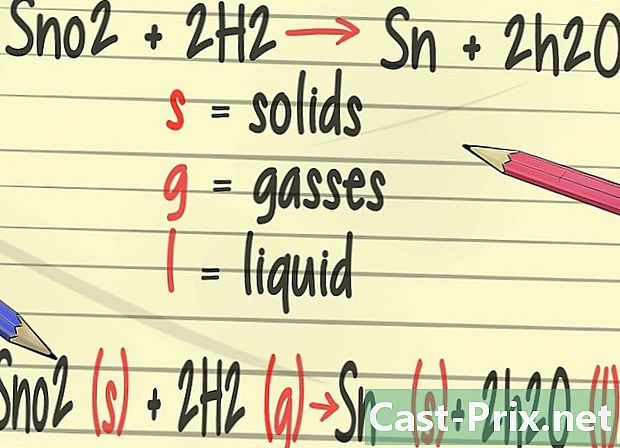
平衡方程式に詳細を追加します。 化学では、元素の物理的状態を表す記号を追加することを学びます。手紙 S 固体、文字を象徴します グラム ガスと手紙に使用されます リットル 液体を表します。 -
反応中に発生する変更を識別します。 化学反応は最初に、基本要素または試薬と呼ばれる既に結合された要素に影響を与えます。 2つ以上の試薬の組み合わせは、1つ以上の製品につながります。- 化学試験に合格するには、試薬、製品を含む方程式を解き、それらの動作に影響する他の要因を考慮することができる必要があります。
-
さまざまな種類の反応を研究します。 化学反応は、単なる成分の組み合わせを超える多くの要因のために発生します。- 化学で研究される典型的な反応は次のとおりです。合成反応、置換、酸塩基反応、酸化還元、燃焼、加水分解、分解、メタセシス、異性化。
- 化学の授業中、教師はプログラムに応じて他のタイプの反応を示すこともあります。明らかに、高校の化学プログラムは、大学で教えられているプログラムほど詳細ではありません。
-

利用可能なすべてのリソースを使用します。 クラスで対処されたフィードバックの各タイプの違いを認識できる必要があります。これらの概念を理解するために必要なすべての学習リソースを使用し、クラスで質問することをheしないでください。- 反応の違いにより、学習者が混乱する場合があり、化学反応中に発生するさまざまなメカニズムを理解することは、コース全体の最も複雑な部分です。
-

化学反応を論理的に理解します。 プロセスをそれ以上に複雑にしないでください。一般的な用語に混乱してしまいます。あなたが勉強するすべての反応において、あなたは何かを何かに変えなければなりません。- たとえば、2分子の水素と酸素の分子を組み合わせることで、水が得られることをすでに知っています。したがって、鍋に水を入れて火にかけると、何かが変わります。実際に化学反応を作成しました。冷凍庫に水を入れると、何かが起こります。つまり、最初の試薬の状態を変更する要因を導入しました。この場合、それは水です。
- あなたがそれを習得するまで、各反応カテゴリーを一つずつ書き直してから、次へ進みます。反応を引き起こすエネルギー源と発生する主要な変化に注目してください。
- これらの概念を理解していない場合は、理解できないすべてのリストを作成して、教師、研究グループ、または化学が得意な人と話し合ってください。
パート4化学への数学の適用
-

基本的な計算のシーケンスを学びます。 化学では、非常に詳細な計算が必要な場合がありますが、基本的な操作で十分な場合もあります。ただし、方程式を完成させて解くには、正確な一連の操作を知ることが不可欠です。- 頭字語を非常に簡単に覚えてください。生徒は特定の概念を暗記するためにさまざまな文を使用し、数学的な操作の順序も例外ではありません。 PEMDASという名前(Maybe My Last ASというフレーズから派生)を使用すると、数学演算を実行する順序を簡単に覚えることができます。各単語の最初の文字は、各操作の順序を示します。最初にすべてを括弧で囲み、次に出展者、乗算、除算、加算、最後に減算を行います。
- PEMDASという名前で示される操作の順序に従って、この式3 + 2 x 2 x 6 = ___の計算を実行します。解決策は15です。
-

非常に大きな値を切り上げる方法を学びます。 化学では丸め数値はあまり一般的ではありませんが、複雑な数学方程式の解が長すぎて記述できない場合があります。取り組んでいる演習の指示を注意深く読んで、答えを丸めるかどうかを確認してください。- 切り上げまたは切り捨てのタイミングを学びます。数値シーケンスでは、次の桁が4以下の場合、切り捨てられます。そして、それが5以上の場合、次の数値に切り上げます。この数字6、66 666 666 666 666 666の例を見てみましょう。小数点第2位まで曲げる必要があるとします。答えは6.67です。
-
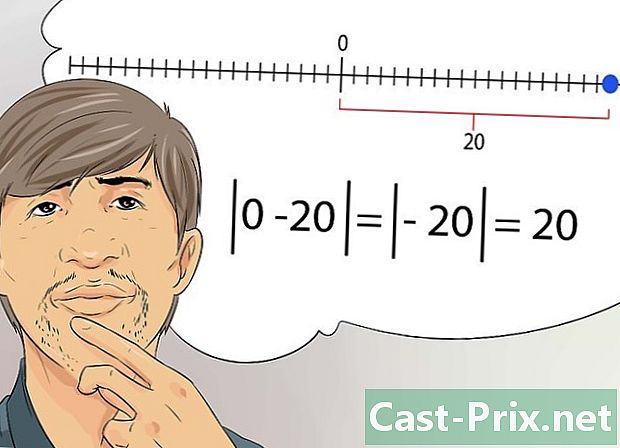
絶対値の概念を理解します。 化学では、いくつかの数値は絶対値と呼ばれ、実際の数学的値ではありません。実数xの絶対値は、この数値xとゼロの間の距離です。- つまり、数値の符号(正または負)を考慮する必要はなくなり、ゼロまでの距離を考慮する必要があります。たとえば、-20の絶対値は20です。
-
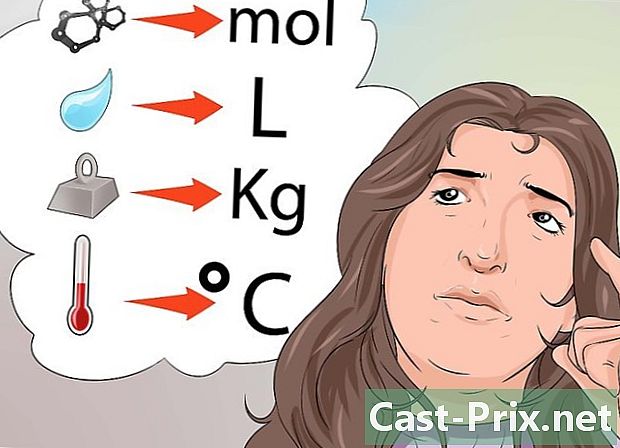
受け入れられている測定単位をよく理解してください。 以下に例を示します。- 材料の量はモル(mol)で表されます。
- 温度は摂氏(°C)、華氏(°F)、またはケルビン(°K)で表されます。
- 質量は、グラム(g)、キログラム(kg)またはミリグラム(mg)で表されます。
- 体積と液体は、リットル(l)またはミリリットル(ml)で表されます。
-

ある測定スケールから別の測定スケールに値を変換する方法を学びます。 化学試験に合格するには、受け入れられているスケールから別のスケールに変換できる必要があります。たとえば、ある温度測定値から別の温度測定値に移動して、キログラムをポンドまたはリットルから液体オンスに変換する必要がある場合があります。- 問題の解決策を元の単位とは異なる測定単位で表現するよう求められる場合があります。たとえば、値が摂氏である温度方程式を解く必要があるが、最終的な答えはケルビンでなければならないとします。
- ケルビンは、化学反応で頻繁に使用される温度測定の国際標準です。摂氏からケルビンまたは華氏に移行する練習をします。
-
エクササイズをするのに時間をかけます。 クラスでいくつかの概念を学習するとき、測定単位をあるシステムから別のシステムに変換する方法を時間をかけて学んでください。 -

濃度の計算方法を学びます。 パーセンテージ、プロポーション、比率の基本的な知識を深めます。 -

栄養表示の練習。 化学試験に合格するには、比率、パーセンテージ、比率、およびそれらの逆演算を簡単に計算できる必要があります。これらの概念をよく理解していない場合は、栄養表示にあるものなど、非常に一般的な他の測定単位でトレーニングする必要があります。- 食品の栄養表示を確認してください。サービングあたりのカロリー、推奨される1日摂取量の割合、総脂肪含有量、脂肪中のカロリーの割合、総炭水化物含有量、さまざまな種類の炭水化物の内訳がわかります。分母として異なるカテゴリの値から異なる割合を計算する方法を学びます。
- たとえば、製品の総脂肪量に対する一価不飽和脂肪の量を計算します。値をパーセンテージに変換します。 1食当たりのカロリー数とパッケージ内のポーションの量を使用して、製品のカロリー数を計算します。包装製品の半分に存在するナトリウムの量を計算します。
- このような変換を使用してトレーニングを行うことにより、使用する測定単位にかかわらず、測定単位を1モルあたりのモル、1モルあたりのグラムなどの化学量に簡単に変換できます。
-

Avogadroの番号の使用方法を学びます。 この定数は、モルに含まれる分子、原子、または粒子の数を表します。 Avogadroの数は6,022 x 1023です。- たとえば、0.450モルのFeにはいくつの原子がありますか?答えは0.450 x 6 022 x 1023です。
-
ニンジンを考えてください。 化学の問題でアボガドロの数を適用するのに問題がある場合は、原子、分子、粒子ではなくニンジンを考えてください。ダースには何個のニンジンがありますか? 12個の要素があるので、12個に12個のニンジンがあります。- さて、この質問に答えてみてください:ほくろの中に何人のニンジンがありますか? 12倍する代わりに、Avogadroの数を使用します。モルには6,022 x 1,023のコアがあります。
- アボガドロの数は、化学量(モル数)をいくつかのオブジェクト(原子、分子、粒子、またはニンジン)に変換するために使用されます。
- 元素のモル数がわかっている場合、Avogadroの定数に問題のモル数を掛けることで、この量の物質に存在する分子、原子、または粒子の数を知ることができます。
- 化学の試験に合格するには、粒子をモルに変換する方法を理解することが重要です。比率とパーセンテージを計算するには、モル換算を行う必要があります。つまり、別の単位と比較して、モルで表された元素の量を知っている必要があります。
-
モル濃度の概念の理解に努めます。 液体媒体に溶解した物質のモル数を考慮してください。これは、モル濃度、つまり1リットルあたりのモル数で表される化学種の割合であるため、理解する上で非常に重要な例です。- 化学では、モル濃度を使用して、液体媒体に含まれる物質の量、または液体溶液に含まれる溶質の量を表します。溶質のモル数を溶液の体積(リットル)で割ることにより、モル濃度を計算できます。その測定単位は、1リットルあたりのモル(mol / l)です。
- 密度を計算します。密度も化学で一般的に使用される尺度です。化学物質の単位体積あたりの質量を表します。ここで最も一般的な測定単位は、1リットルあたりのグラム(g / l)または1立方センチメートルあたりのグラム(g / cm3)です。
-

方程式を実験式に簡約します。 つまり、方程式を最も単純な形式に縮小しないと、方程式の最終的な解は間違っていると見なされます。- このタイプの説明は、分子を構成する化学元素間の正確な比率を示すため、これは分子式には適用されません。
-

分子式の概念を理解します。 分子式を分子の組成を正確に表現するため、分子式を最も単純な形式または経験的な式に還元する必要はありません。- 体の分子式を書くことは、化学元素の略語と分子内の各元素の原子数を使用することです。
- 水の分子式、H2Oを想定します。水の各分子は、2つの水素原子と1つの酸素原子で構成されています。ラセタミノフェンの分子式、C8H9NO2でも同じことを試してください。実際、すべての化合物は分子式で表されます。
-

化学量論の詳細をご覧ください。 あなたはおそらくこの言葉に出会うでしょう。化学量論は、数式を使用した化学反応の定量的割合の研究です。化学量論(化学に適用される数学)では、元素および化合物の値は通常、モル、モル百分率、1リットルあたりのモル、または1キログラムあたりのモルで表されます。- 最も一般的な数学的操作の1つは、グラムをモルに変換することです。通常、グラムで表される元素の原子質量単位は、この物質の1モルに相当します。たとえば、カルシウムラトームの質量は40原子質量単位です。したがって、40 gのカルシウムは1モルのカルシウムに相当します。
-

追加のエクササイズについては先生にお尋ねください。 数式と変換が問題になる場合は、先生に相談してください。使用するすべての概念を明確に理解するまで、自分で行うための演習をさらに行うように彼に依頼します。
パート5化学の言語を使用する
-
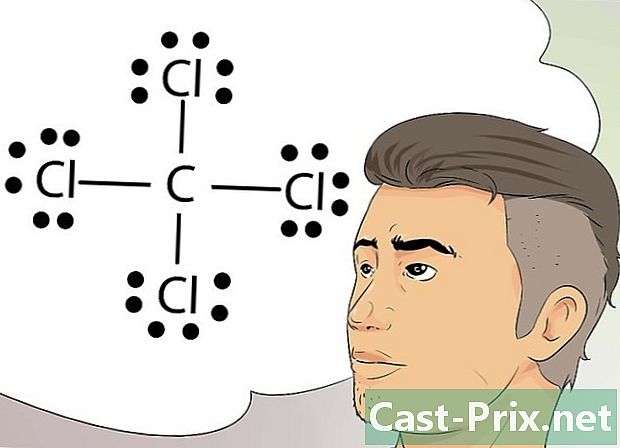
ルイスの構造を認識してください。 これらの構造は、ルイス式とも呼ばれ、ドットを使用して原子の外層にあるグループ化された電子と単一電子を表すグラフィカルな表現です。- これらの構造は、単純な図を描き、共有結合など、原子または分子内でいくつかの要素が共有する結合を識別するのに非常に役立ちます。
-

ロクテットルールを学びます。 ルイスの構造はこの規則に基づいており、原子の外層に正確に8個の電子が含まれている場合、原子は安定していると述べています。この規則の例外として、水素はその外側の層に2つの電子があると安定していると見なされます。 -
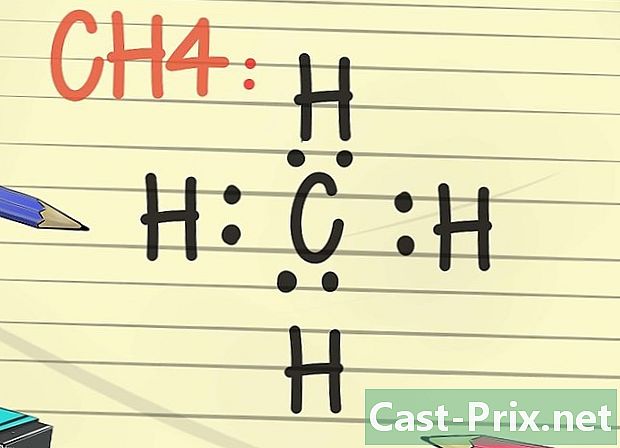
ルイス構造を描きます。 この構造は、一連のポイントで囲まれた要素のシンボルで表されます。それが映画のキャプチャされた静止画像だと想像してください。電子が核の周りに引き寄せられるのではなく、与えられた瞬間の位置を表します。- ルイス構造により、電子の最も安定した配置、別の化学元素との接続位置を視覚化できます。また、結合強度に関する情報(共有結合か二重結合かなど)も提供します。
- バイト規則を考慮して、ルイス炭素構造(C)を描画してみてください。次に、ラトームの両側に2つのポイントを配置します(上下左右)。次に、各ドットペアの反対側にH、水素ラトームシンボルを書き込みます。このルイス構造は、4つの水素原子に囲まれた炭素原子を表します。電子が共有結合で接続されている場合、炭素が各水素原子と電子を共有していることを意味し、これは水素にも適用されます。
- この例の分子式は、メタンのCH4です。
-
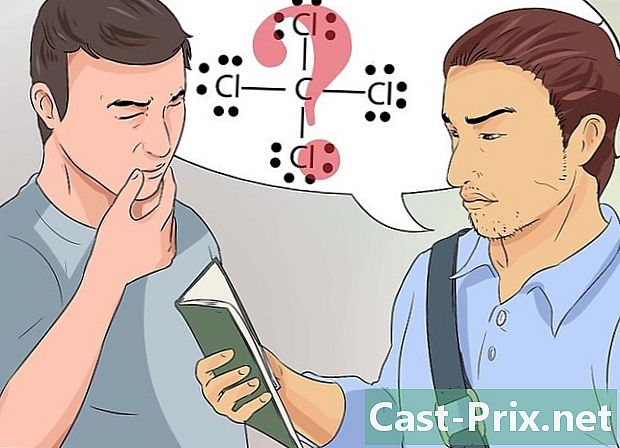
結合に従って電子を配置する方法を学びます。 ルイス構造は、化学結合の単純な視覚的表現です。- 化学結合やルイス式に関する特定の概念を理解していない場合は、教師または研究グループと話し合ってください。
-
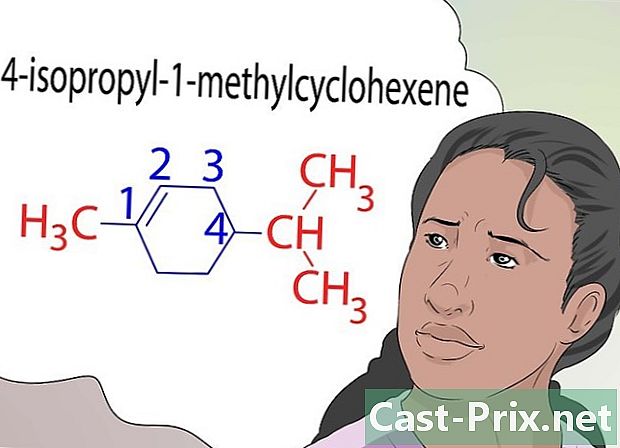
化合物に名前を付ける方法を学びます。 化学には、命名法に関する独自のルールがあります。化合物で起こる反応の種類、外層への電子の損失または追加、および化合物の安定性または不安定性は、化合物に名前を付けることを可能にする要因です。 -

化学の命名法を過小評価しないでください。 ほとんどの場合、化学の最初の章は命名法に焦点を当てています。多くの場合、化合物の誤認により、レビューに失敗する可能性があります。- 可能であれば、コースを開始する前に化合物の命名方法を学習します。ガイドを購入するか、オンラインでリソースを参照できます。
-
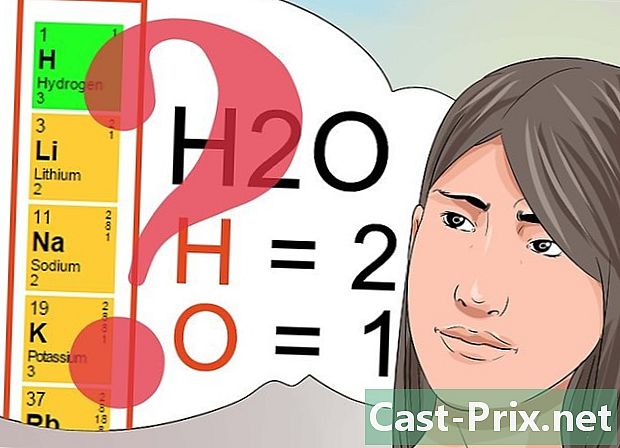
上付き文字と下付き文字の数字の意味を理解します。 試験に合格する場合は、これらの数値の意味を理解することが重要です。- 上付きの数字は、周期表に表示されるパターンに従い、化学元素または化合物の総電荷を示します。周期表を繰り返すと、同じ垂直列(グループ)に沿って配置された要素が指数で同じ番号を共有していることがわかります。
- インデントされた数字は、化合物の一部として識別される各要素の量を決定するために使用されます。上記のように、分子H2Oのインデックス2は、2つの水素原子があることを示しています。
-

原子が互いにどのように反応するかを発見してください。 化学で使用される命名法の一部には、特定の種類の反応から生じる製品の命名に関する特定の規則が含まれています。- これらの反応の1つは、酸化還元反応です。これは、電子が取得または失われる反応です。
- ドキシドレダクション反応中に発生するメカニズムを覚えて、名前を暗記する RROO。それを覚える簡単な方法です 還元剤は電子を生成し、酸化剤は.
-
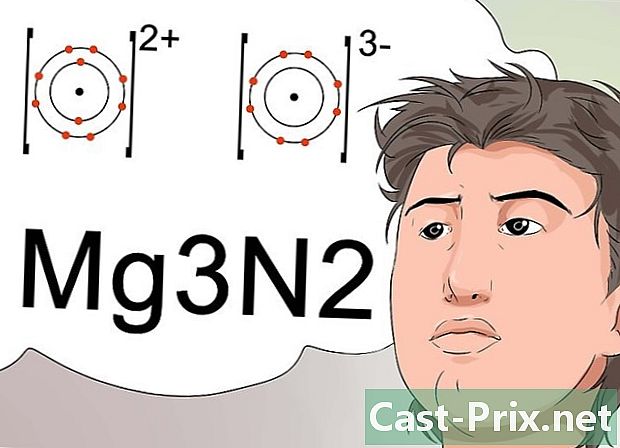
手がかりの数字を使用して、中性分子を取得します。 科学者は手がかりを使用して化合物の決定的な分子式を特定し、これは化合物が中性電荷で安定していることも示しています。- 安定した電子構成に到達するには、陽イオン(陽イオン)を同じ強度の陰イオン(陰イオン)で補正する必要があります。出展者は負荷を表します。
- たとえば、ライオンのマグネシウムには+2の正電荷が、ライオンの窒素には-3の負電荷があります。数字の+2と-3は上付き文字で配置する必要があります。 2つの元素を適切に組み合わせて中性分子を得るには、2つの窒素原子に3つのマグネシウム原子を使用する必要があります。
- したがって、得られる分子はMg3N2です。
-
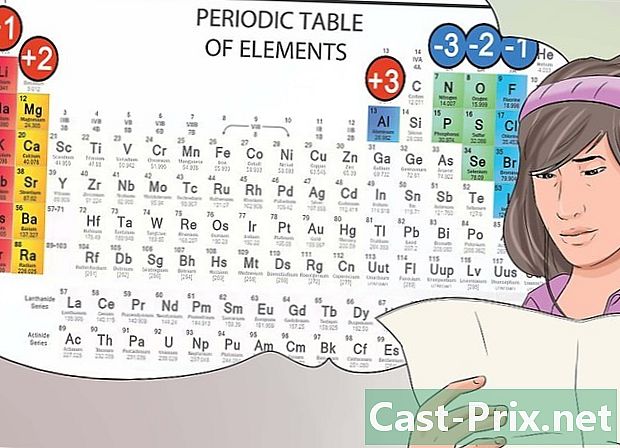
アニオンとカチオンをその位置から特定します。 周期表では、最初のグループに属する元素はアルカリ金属と見なされ、+ 1の正電荷を持ちます。ナトリウム(Na +)およびリチウム(Li +)は例です。- アルカリ土類金属は2番目のグループの一部であり、マグネシウム(Mg2 +)やバリウム(Ba2 +)などの2+カチオンを形成します。
- 周期表の7番目の列に属する化学元素は、ハロゲンのファミリーを構成し、負電荷を持つ陰イオン(塩素(Cl-)や陰イオン(I-)など)を形成します。
-

最も一般的な陽イオンと陰イオンを認識します。 化学試験で成功するには、指数の数値が変化しない要素のグループの命名法を可能な限り知る必要があります。- つまり、マグネシウムは常にMgで表され、常に+2の正電荷を持ちます。
-

情報に圧倒されないようにしてください。 さまざまな化学反応、電子交換、元素または化合物の電荷の変化に関するすべての詳細情報を理解して覚えることは容易ではありません。- 理解できないトピックを説明的な用語で表現します。たとえば、酸化反応を理解していない場合、または元素がどのように負電荷と正電荷と結合するかを理解していない場合は、そう言います。自分にとって問題のある概念や概念を明確に表現することで、物事をたくさんコントロールできることに気付くかもしれません。
-

定期的に先生に会います。 理解できないトピックのリストを作成し、先生に助けを求めてください。さらに複雑で理解しにくい教室の概念を入力する前に、複雑な概念を吸収する機会です。 -

新しい言語を学んでいることを自覚してください。 電荷、分子内の原子数、および分子間に形成される結合を示すために書かれた式は、化学の言語の一部であることを理解してください。これは、視覚的に表現する方法であり、化学反応中に発生するさまざまな変換を記述する際に使用できますが、これは見ることはできません。- すべてのメカニズムを肉眼で観察できれば、化学を理解するのははるかに簡単です。ただし、反応のメカニズムだけでなく、現象を記述するために化学で使用される用語を理解するよう努力する必要があります。
- 化学のクラスを理解するのが難しい場合は、あなたが一人ではないことを知ってください。しかし、だまされてはいけません。先生と話をしたり、グループで勉強したり、先生のアシスタントに連絡したり、化学が本当に得意な人に助けを求めたりしてください。コース全体を学ぶことができますが、特定の章をよりよく理解するために説明できるように、助けを求めるのは良いことです。