酸化の数を見つける方法
著者:
Roger Morrison
作成日:
27 9月 2021
更新日:
1 J 2024

コンテンツ
この記事の内容:化学ルールから酸化数を決定する特定のルールに従っていない原子の酸化数を決定する
化学では、「酸化」および「還元」という用語は、原子(または原子群)がそれぞれ電子を失ったり獲得したりする反応を指します。酸化番号は、原子(または原子のグループ)に割り当てられた番号で、化学者が転送できる電子の数と、反応中に試薬が酸化または還元を受けるかどうかを知るのに役立ちます。原子に原子番号を割り当てるプロセスは、原子の電荷と原子が属する分子の化学組成に応じて、単純から非常に複雑になる可能性があります。問題をさらに複雑にするために、一部の原子は3つ以上の酸化数を持つ場合があります。幸いなことに、酸化数の決定は、化学と代数の知識があると便利かもしれませんが、実装しやすい明確なルールによって管理されます。
ステージ
パート1化学ルールから酸化数を決定する
-

作業している製品が元素原子かどうかを確認します。 自由で他の元素と結合していない元素原子の酸化数は常に0です。これは、元素形態がこの単純な原子で構成される原子だけでなく、元素形態の原子にも当てはまります。二原子または多原子です。- たとえば、Al(S) とCl2 両方とも元素の結合されていない形であるため、両方の酸化数は0です。
- 硫黄の元素形態、S8、またはオクタ硫黄は、不規則ですが、酸化数も0です。
-

問題の製品がイオン化されているかどうかを確認します。 イオンの酸化数はそれらの電荷に等しい。これは、他の元素にリンクされていないイオンだけでなく、イオン化合物の一部であるイオンにも当てはまります。- たとえば、Clイオンの酸化数は-1です。
- Clイオンは 常に NaCl化合物の一部である場合、酸化数-1。定義上、Naイオンの電荷は+1であるため、Clイオンの電荷は-1であることがわかります。したがって、その酸化数は常に-1です。
-

金属イオンの場合、いくつかの酸化数があります。 多くの金属要素には複数の負荷があります。たとえば、鉄(Fe)は、+ 2または+3の電荷を持つイオン化された形である場合があります。金属イオンの電荷(したがって、それらの酸化数)は、それらが含まれる化合物の他の原子の電荷の関数として、または情報がeの形式で書き込まれるときにローマ数字を使用して決定できます(文中:「鉄イオン(III)の電荷は+3」)。- アルミニウム金属イオンを含む化合物の例を見てみましょう。 AlCl化合物3 全体の電荷は0です。Clイオンの電荷は-1であり、化合物には3があるため、Alイオンの電荷は+3でなければならないため、全体の電荷はすべてのイオンのαは0です。したがって、Alの酸化数は+3です。
-

酸素に-2の酸化数を割り当てます(例外を含む)。 で ほとんどの 場合によっては、酸素原子の酸化数は-2です。ただし、この規則にはいくつかの例外があります。- 酸素が元素状態(O2)、すべての元素原子の場合と同様に、その酸化数は0です。
- 酸素が 過酸化物、その酸化数は-1です。過酸化物は、単純な酸素-酸素(または過酸化物アニオン)結合を持つ化合物のクラスです2)。たとえば、Hの分子では2O2 (過酸化水素)、酸素の酸化数(およびその電荷)は-1です。
- 酸素がフッ素に結合すると、その酸化数は+2になります。詳細については、この記事で後述するフッ化物のルールをお読みください。
-
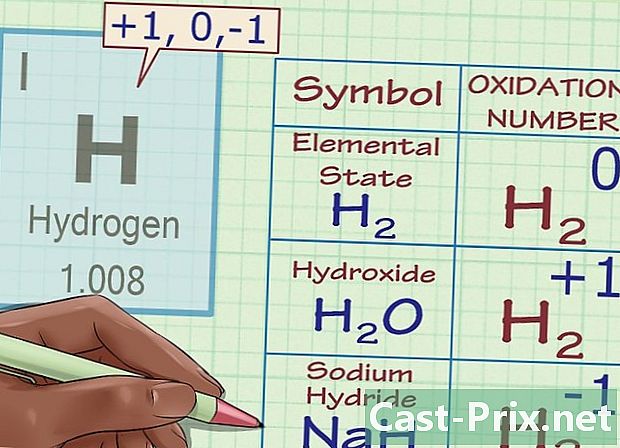
(例外を除いて)水素に+1の酸化数を割り当てます。 酸素に関しては、水素の酸化回数は例外的な場合があります。一般に、水素の酸化の数は+1です(ただし、水素が元素の形である場合を除きます。H2)。ただし、特殊ないわゆるハイブリッド化合物の場合、水素の酸化数は-1です。- たとえば、Hの分子では2O、酸素は-2の電荷を持っているため、水素の酸化数は+1であり、化合物の総電荷が0になるには2 +1の電荷が必要であることがわかっています。ただし、水酸化ナトリウムNaHのハイブリッド型では、Naイオンの電荷が+1であるため、水素の酸化数は-1です。したがって、化合物の総電荷がゼロになるためには、水素電荷(およびその酸化数)が-1に等しくなければなりません。
-

Fluorは 常に -1の酸化数 すでに述べたように、特定の元素の酸化の数は、多くの理由で異なります(これは、金属イオン、過酸化物の酸素原子などの場合です)。ただし、フッ素の酸化数は-1であり、これは決して変化しません。これは、フッ素が最も電気陰性度の高い元素であるという事実によるものです。言い換えると、フッ素は、電子の1つを与える可能性が最も低く、引き継ぐ可能性が最も高い元素です。別の要素の電子。それが彼の請求が変わらない理由です。 -

化合物の酸化数は、その化合物の電荷に等しいと考えてください。 化合物のすべての原子の酸化数の合計は、この化合物の電荷と等しくなければなりません。たとえば、化合物が帯電していない場合、その原子すべての酸化数の合計は0に等しくなければなりません。化合物が多原子電荷イオン-1の場合、酸化数の合計は-1である必要があります。- これは、あなたの仕事がうまくいったかどうかをチェックする良い方法です-もしあなたの化合物の酸化数の合計があなたの化合物の総電荷と等しくなければ、間違いを犯したと確信できます。どこかであなたの酸化数を決定します。
パート2特定の規則に従わない原子の酸化数を決定する
-

酸化数を割り当てるための規則がない原子を見つけます。 原子によっては、酸化数を決定するための特定のルールがありません。前の段落に原子が表示されず、その電荷がわからない場合(たとえば、大きな化合物の一部であり、個々の電荷が与えられていない場合)、次のことができます。除去を進めることにより、原子の酸化の数を見つけます。最初に、化合物の総電荷に基づいて関心のある原子の数を決定する前に、化合物の他の各原子の酸化数を決定します。- たとえば、Na化合物では2SO4、硫黄(S)の電荷は不明です。つまり、元素の形ではないため、電荷は0とは異なるということしか言えません。酸化数を決定するこの代数的方法を適用することは良い候補です。
-

化合物の他の元素の酸化数を見つけます。 酸化数を決定するための化学ルールを使用して、化合物の他の原子の酸化数を見つけます。 O、H原子などの例外的なケースに注意してください。- 前のセクションで概説した化学規則に従って、Na化合物では2SO4 Naイオンの電荷(したがって酸化数)は+1であり、酸素原子の酸化数は-2です。
-

各原子について、その数に酸化数を掛けます。 対象の原子を除くすべての原子の酸化数がわかったので、これらの原子の一部が化合物に複数回出現する可能性があることを考慮する必要があります。各原子の数値係数(化合物内の原子の化学記号の後にインデックスで記述)にその酸化数を掛けます。- Na化合物で2SO4Naの原子が2つ、Oの原子が4つあることがわかっています。そのため、+ 1(Naの酸化の数)に2を掛けて2の結果を取得し、-2(2の数O)を4酸化して-8の結果を得る。
-
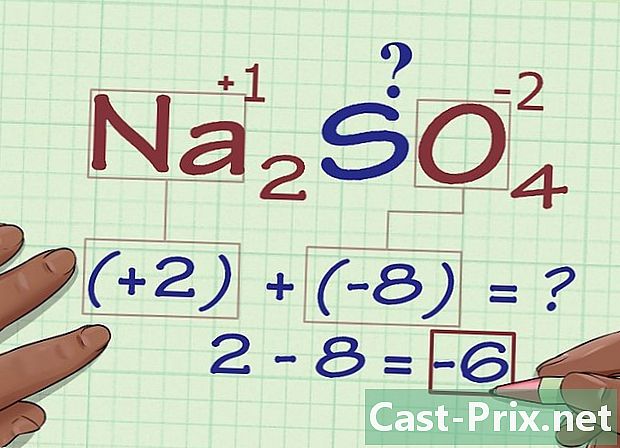
結果を追加します。 乗算の結果を追加して酸化数を取得します 無し 興味のある原子の酸化数を考慮に入れてください。- Naの例では2SO4、-6を取得するには2と-8を追加する必要があります。
-
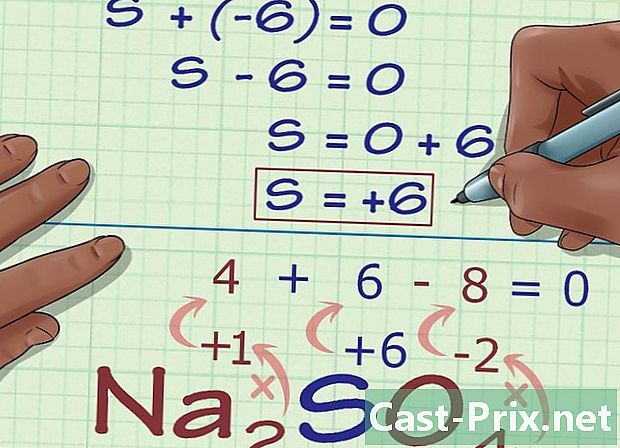
化合物の電荷に基づいて未知の酸化数を計算します。 これで、単純な代数規則を使用して、興味のある酸化数を見つけるために必要なすべての情報が得られました。前のステップの結果に未知の酸化数を加えたものが、化合物の総電荷量に等しくなる方程式を確立します。言い換えれば: (既知の酸化数の合計)+(未知の酸化数)=(化合物の電荷)。- Naの例をとって2SO4方法は次のとおりです。
- (既知の酸化数の合計)+(未知の酸化数)=(化合物の電荷)
- -6 + S = 0
- S = 0 + 6
- S =6。Sの酸化数は 6 Na化合物で2SO4.
- Naの例をとって2SO4方法は次のとおりです。

